
Научный коллектив Института экспериментальной медицины (ИЭМ) НМИЦ им. В. А. Алмазова под руководством д.м.н., члена-корреспондента РАН Михаила Михайловича Галагудзы установил возможность уменьшения размеров зоны некроза миокарда при моделировании инфаркта в остром эксперименте у крыс на фоне синдрома системного воспалительного ответа (ССВО) за счет лечебно-профилактического введения в рацион смеси бифидо- и лактобактерий. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журналах Microorganisms, «Медицинская иммунология», «Бюллетене экспериментальной биологии и медицины», «Российском физиологическом журнале им. И. М. Сеченова» и др.
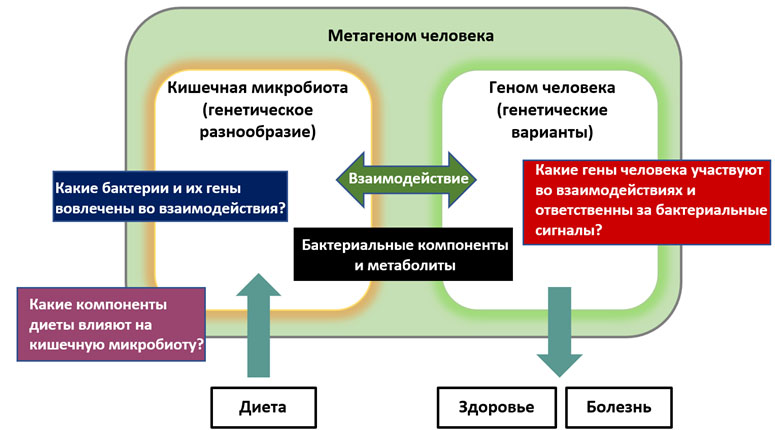
Геном человека состоит из 22 тысяч генов, кодирующих белки для обслуживания нашего метаболизма, тогда как микробиом привносит, по разным оценкам, в 150–360 раз большее количество уникальных кодирующих генов, чем собственно человеческих. В этой связи ученым представляется обоснованным, что иммунологический и метаболический потенциал микробиоты кишечника может иметь непосредственное отношение, в том числе, и к модулированию резистентности миокарда к ишемическому реперфузионному повреждению. Исследователи предполагают, что симбиотические микроорганизмы, на основе которых разрабатываются пробиотические препараты, существенно влияют как на течение нормальных физиологических процессов, так и при патологических состояниях, в особенности воспалительной природы.
«Эволюционно адаптированные пробиотические микробы жизненно заинтересованы в сохранении взаимовыгодных отношений с хозяином. Мы предполагаем, что бактерии защищают клетки сердца от токсического повреждения и последствий кислородного голодания через тонкую регуляцию про- и противовоспалительных сигнальных молекул», — пояснил директор Института экспериментальной медицины НМИЦ им. В. А. Алмазова Михаил Михайлович Галагудза.
Для определения кардиопротективных возможностей пробиотических микроорганизмов была разработана оригинальная экспериментальная модель полиморбидности на мелких грызунах, включающая первичное висцеральное ожирение (ПВО), воспалительное заболевание толстой кишки (ВЗТК) и антибиотико-индуцированный дисбиоз (АИД). Данный букет патологий, широко распространенный в клинике, у экспериментальных животных характеризовался существенным увеличением показателей ряда провоспалительных цитокинов.
За несколько дней до моделирования инфаркта миокарда и АИД в остром эксперименте и далее в течение 8 дней разным группам крыс с ПВО внутрижелудочно вводили различные пробиотические штаммы и смеси штаммов.
Наблюдения показали, что введение смеси Lactobacillus acidophilus и Bifidobacterium animalis, в отличие от других пробиотиков, на 10 % уменьшило размеры повреждений сердечной мышцы, вызванных инфарктом. Это улучшение в состоянии здоровья сердца животных сопровождалось снижением концентрации провоспалительных цитокинов и улучшением общего состояния организма, в том числе пищеварительной системы.
Как предполагают ученые, в основе механизма кардиопротекции лежит способность симбиотических микроорганизмов синтезировать блокаторы некоторых провоспалительных цитокинов, рецепторов к ним либо модулировать экспрессию их генов. Дальнейшее изучение механизмов пробиотической кардиопротекции, как надеются исследователи, поможет создать новые лечебно-профилактические подходы в кардиологии путем подбора штаммов для новых лекарственных пробиотических препаратов и продуктов функционального питания.
Новость в СМИ:
Вечерний Санкт-Петербург
Телеканал Санкт-Петербург
Диалог
78.ru
Naked Science
Научная Россия
МИР 24
Автопарус
