Институт онкологии и гематологии
Институт онкологии и гематологии Центра Алмазова объединяет научные подразделения, проводящие фундаментальные и трансляционные исследования в области гематологии, трансфузиологии, ревматологии и инфекционных заболеваний.
Руководителем института с момента его основания является профессор А. Ю. Зарицкий. Институт онкологии и гематологии тесно сотрудничает с ведущими научными и клиническими учреждениями России и зарубежья в области науки, образования и клиники.
Клинические исследования
Калькулятор CIRS-G
Исследование IB-RU-SCOPE — ибрутиниб в лечении хронического лимфолейкоза в России
История создания института
Институт был организован в 2009 году как Институт гематологии под руководством проф. А. Ю. Зарицкого — одного из ведущих ученых в области изучения биологии лейкемических клеток, корифея российской клинической гематологии. Предпосылками к созданию Института, объединяющего научные подразделения молекулярно-биологического, гематологического, трансфузиологического, инфекционного, патоморфологического и ревматологического профиля, послужили исследования ряда ключевых сотрудников, а также общее стремление развиваться в соответствии с принципами трансляционной медицины.
С момента основания Института основными направлениями научного поиска были изучение биологии гематологических, ревматологических и инфекционных заболеваний, механизмов резистентности к современной терапии, разработка методик, улучшающих диагностику и прогнозирование течения различных заболеваний. Финансирование исследований Института осуществляется за счет нескольких государственных заданий, грантов РФФИ, а также в рамках международного сотрудничества. Результатом работы явились более сотни публикаций в российских и международных журналах.
Наиболее существенная реорганизация Института произошла в 2019 году, когда с появлением в Центре Алмазова клинических подразделений, занимающихся солидной онкологией, возникла необходимость в создании научных структур соответствующего профиля. В результате Институт гематологии был преобразован в Институт онкологии и гематологии с формированием нескольких новых подразделений, задачей которых является изучение механизмов возникновения и развития солидных опухолей, а также оптимизация методов диагностики и лечения последних.
В структуру Института вошли 3 научно-исследовательских отдела с 6 научно-исследовательскими лабораториями и 3 научными группами. В частности, для изучения биологии солидных опухолей и усовершенствования методов их морфологической, иммуногистохимической, а также молекулярно-генетической диагностики создан отдел фундаментальной онкологии. Был создан научно-исследовательский отдел ядерной медицины и тераностики под руководством проф. Д. В. Рыжковой. Лаборатории имеют международные сертификаты и дипломы.
В настоящее время в составе Института научную, образовательную и клиническую деятельность ведут 5 докторов (из них 4 профессора) и 7 кандидатов наук.
Всего в Институте 55 штатных единиц, из них научных ставок: 2 – главного научного сотрудника, 6,5 – ведущего научного сотрудников, 8,5 – старшего научного сотрудника, 14 – научного сотрудника, 14,5 – младшего научного сотрудника.
Основные направления деятельности
- Иммунотерапия онкологических и онкогематологических больных, в том числе с использованием метода CAR-T.
- Таргетная терапия лимфо- и миелопролиферативных заболеваний.
- Стволовые гемопоэтические клетки для терапии онкологических больных.
- Кинетика лейкемических клеток при остром миелобластном лейкозе.
- Опухоли ЦНС у детей младшего возраста;
22 сентября 2020 года Онлайн-школа для врачей и пациентов с хроническим миелоидным лейкозом
В Центре Алмазова создана лаборатория генной инженерии и клеточной терапии
Ученые Центра Алмазова создали собственный модуль синтеза радиофармацевтических препаратов
CAR-T терапия: как стать доступной в России?
Специалисты Центра Алмазова отмечены премией Всероссийского союза пациентов
В Санкт-Петербурге прошла школа пациентов с ХМПЗ
Сотрудники Центра Алмазова приняли участие в Конгрессе SOHO
Доклад о разработке CAR-T клеток для лечения опухолей награжден дипломом III степени
Благодарность от врачей Хабаровского края
Проблемная комиссия института
Проблемная комиссия по гематологии, онкологии и ревматологии. Подробнее
Структура института
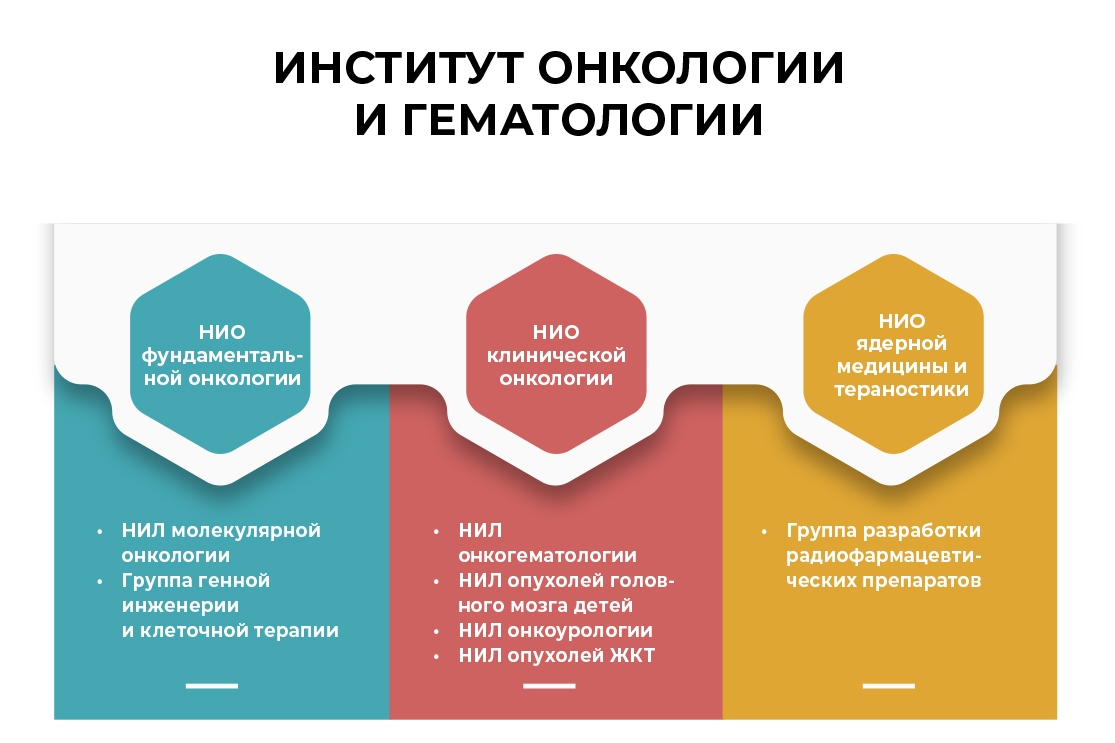
- НИО клинической онкологии с лабораторией онкогематологии
- НИО фундаментальной онкологии с группой генной инженерии и клеточной терапии
- НИО ядерной медицины и тераностики с группой разработки новых радиофармацевтических препаратов
Основные технологии Института
- Изучение костномозговой ниши и биологии гемопоэтических столовых клеток.
- Клеточная терапия и CAR-T лимфоциты.
- Изучение новых прогностических маркеров и оптимизация схем терапии.
- Внедрение новых препаратов.
- Логическим продолжением исследований проф. А. Ю. Зарицкого явилась работа по изучению костномозговой ниши гемопоэтических стволовых клеток (ГСК), в частности, мезенхимных стромальных клеток (МСК). Данные работы проводятся в институте с момента его основания. В разное время темой ГСК занимались научные сотрудники П. А. Бутылин, М. В. Пузанов, С. В. Анисимов, С. В. Жук, О. В. Кулемина, И. А. Мельн.Данной теме посвящено несколько публикаций в ведущих российских гематологических журналах. Так, в 2012 году было показано, что совместное культивирование ГСК и МСК, трансдуцированных геном DLL1, увеличивает экспансию малодифференцированной фракции CD34+ клеток, была разработана модель сосудистой ниши костного мозга (эндотелиальные клетки с конститутивно активным AKT1), показана роль гипоксии в сохранении примитивной фракции CD34+CD38- клеток и высокой клоногенной способности ГСК и т.д.
- НИОКР в области трансплантации гемопоэтических стволовых клеток проводятся под руководством Д.В. Моторина. С 2009 года в клинические подразделения успешно внедрена методика аутологичной трансплантации ГСК, с 2011 года – аллогенной родственной, с 2015 года – гаплоидентичной трансплантации ГСК. За прошедшие годы накоплен большой практический опыт и собран значительный объем теоретических данных по эффективности ТГСК при различных гемобластозах. С 2018 года инициированы исследования по изучению иммунологической реконституции после аллогенной ТГСК, которые продолжаются в рамках ГЗ до настоящего времени.В настоящее время крайне перспективным направлением в онкологии является терапия генетически модифицированными Т-клетками, экспрессирующими химерный антигенный рецептор (CAR-T). Работы по созданию CAR-T клеток в Институте проводятся с 2013 года (С.В. Жук). В 2017 году сотрудниками НИЛ онкогематологии были получены первые собственные Т-лимфоциты, обладающие цитотоксическим действием в отношении клеток, несущих на своей поверхности CD19. Результаты работы были представлены на конференции «Злокачественные лимфомы» в октябре 2017 года, доклад был награжден дипломом.
- В рамках нескольких государственных заданий Министерства здравоохранения Российской Федерации с 2011 года институт проводил НИОКР по открытию и изучению новых прогностических маркеров течения гемобластозов, созданию клинических рекомендаций по оптимальной терапии этих заболеваний. Так, интересные результаты были получены при изучении значимости экспрессии гена WT1 при миелопролиферативных заболеваниях (Н.Т. Сиордия). Было выявлено, что WT1 может быть высокоспецифичным и высокочувствительным молекулярным маркером для дифференциальной диагностики между миелофиброзом истинной полицитемией/эссенциальным тромбоцитозом. Он также может быть использован для верификации трансформации этих заболеваний в миелофиброз. Предварительные данные подтвердили, что этот маркер может быть использован также и для прогнозирования прогрессии болезни. В настоящее время продолжается изучение корреляции динамики уровня экспрессии данного гена и опухолевой массы на фоне терапии ингибиторами тирозинкиназ при миелофиброзе.Изучение динамики уровня экспрессии WT1, а также других молекулярных маркеров, таких как BAALC, DNMT3A, RUNX1-RUNX1T1 при острых миелобластных лейкозах позволило определить прогностически значимые степени редукции транскриптов данных генов в постиндукционном периоде. Также выявлена значимость мониторинга уровня экспрессии данных генов у пациентов в клинико-гематологической ремиссии. Результатом этой работы явилась защита кандидатской диссертации Л. Л. Гиршовой в 2018 году.Изучение мутаций генов TP53, NOTCH1, оценка мутационного статуса IGHV-генов, а также изучение других молекулярно-генетических аберраций (del17p, del11q) при хроническом лимфолейкозе позволило оценить их прогностическую значимость при современной стандартной терапии по схеме «бендамустин+ритуксимаб». В этой работе также оценивалась роль мониторинга минимальной остаточной болезни с использованием уровня экспрессии CD38+ клеток на отдаленные результаты терапии.Изучение роли молекулярных маркеров при лимфоидных и миелоидных новообразованиях является приоритетным направлением работы института гематологии. Эти работы позволяют оптимизировать ведение пациента, включая выбор наиболее эффективных режимов терапии, инновационных препаратов, а также своевременно направить пациента на аллогенную трансплантацию гемопоэтических стволовых клеток.
- С момента основания Институт принимает активное участие во внедрении новых препаратов для лечения различных онкогематологических заболеваний, в первую очередь хронического миелолейкоза (напр., первый отечественный ингибитор BCR/ABL PF-114), Ph-негативных миелопролиферативных заболеваний (руксолитиниб, федратиниб, отечественный пегилированный интерферон), хронического лимфолейкоза (бендамустин, ибрутиниб, венетоклакс) и острых миелобластных лейкозов (ингибиторы FLT3, Hedgehog).Большинство гемобластозов, в том числе хронический миелолейкоз и хронический лимфолейкоз, являются орфанными заболеваниями и, следовательно, адекватное изучение этих заболеваний, а также факторов, влияющих на эффективность терапии, требует коопераций усилий ученых и врачей многих научных и лечебных учреждений. Поэтому институт активно сотрудничает с ведущими гематологическими клиниками России, организуя и проводя ретроспективные и проспективные клинические исследования.Например, в 2011 году в терапевтическом арсенале против ХЛЛ появился препарат бендамустин — новый эффективный и малотоксичный алкилатор. Уже в 2012—2016 гг. при поддержке фармацевтической компании Астеллас Институт провел широкомасштабное клиническое исследование препарата на базе 34 специализированных гематологических центров, расположенных в 26 городах России (BEN-001 “Norma”) при участии Е. А. Стадник. В рамках этого исследования была изучена эффективность и безопасность комбинации «бендамустин + ритуксимаб» у ранее нелеченых больных ХЛЛ. Важной научной частью этого исследования был поиск молекулярных прогностических факторов течения заболевания. Фактически, BEN-001 стало первым многоцентровым российским клиническим исследованием в области ХЛЛ такого масштаба. В рамках исследования на базе структурных подразделений Института выполнялся ряд высокотехнологичных анализов, в том числе определение мутационного статуса IGHV-генов (А. М. Румянцев), оценка минимальной остаточной болезни методом проточной цитометрии (Ю. В. Миролюбова) и цитогенетические исследования (Т. С. Никулина). Результаты исследования были опубликованы в 2017 году в ведущем отечественном гематологическом журнале.С 2019 года институт проводит проспективное наблюдательное исследование IB-RU-SCOPE, в котором проводится анализ эффективности и безопасности ингибитора Btk ибрутиниба при ХЛЛ в условиях обычной клинической практики. В последние годы аналогичные исследования инициированы в области ОМЛ и хронических миелопролиферативных заболеваний.
Сотрудничество
Институт активно сотрудничает с международной организацией European LeukemiaNet, которая была создана в 2004 году при поддержке 6-ой рамочной программы Европейского Союза. Преимущественно работа с ELN концентрировалась в области изучения заболеваемости и эффективности лечения хронического миелолейкоза в различных регионах России. Директор Института А. Ю. Зарицкий являлся главным исследователем в крупном проекте «The EUropean Treatment Outcome Study (EUTOS) for CML». В проекте «Ретроспективный регистр пациентов с хроническим миелолейкозом Северо-Западного региона России» Институт активно сотрудничал с ведущими гематологическими клиниками Санкт-Петербурга, Ленинградской области, Республики Коми, Республики Карелия и Мурманской области.
Работа по данному проекту была успешно завершена в 2011 году. В проекте «Проспективный регистр пациентов с хроническим миелолейкозом Санкт-Петербурга и Ленинградской области» по созданию популяционной базы данных больных хроническим миелолейкозом было продолжено плодотворное сотрудничество со всеми гематологическими клиниками Санкт-Петербурга и Ленинградской области (РосНИИ гематологии и трансфузиологии, СПбГМУ им. И. П. Павлова, Городская больница № 15, Городская клиническая больница № 31). Активное участие проф. А. Ю. Зарицкого и Е. Г. Ломаиа в программах EUTOS и других проектах European LeukemiaNet привели к нескольким совместным публикациям и неоднократно отмечалось грамотами ELN.
В 2011 году лаборатория молекулярной генетики ЦКДЛ совместно с НИЛ онкогематологии, выступая референс-лабораторией, первой в Российской Федерации завершила процесс стандартизации молекулярного метода количественного определения экспрессии гена BCR/ABL у больных хроническим миелолейкозом. Проведение данной работы осуществлялось совместно с European LeukemiaNet. Результаты этой работы в настоящее время позволяют осуществлять мониторинг минимальной остаточной болезни у данных пациентов, сопоставляя получаемые результаты с европейскими стандартами, а значит своевременно менять лечебную тактику.
 |
 |
| Подписание договора о сотрудничестве между Центром Алмазова (проф. А. О. Конради, проф. А. Ю. Зарицкий) и Cancer Center (Dr. Anderson). |
|
Подтверждением успешного завершения данного процесса является получение международного сертификата.



Сотрудничество с ELN в области ХЛЛ в рамках Европейской инициативы по изучению ХЛЛ (ERIC) позволило стандартизировать методику определения мутационного статуса IGHV-генов и наладить анализ мутаций гена TP53 у больных ХЛЛ на базе лабораторий Центра. Соответствующие сертификаты ERIC были получены в 2017 году.
Сотрудничество в рамках ERIC продолжается до настоящего времени, но уже в сфере изучения механизмов резистентности к новым таргетным препаратам – ингибиторам BTK и Bcl2 (В. В. Стругов).
Сотрудничество с MD Anderson Cancer Center
Контакты с MD Anderson Cancer Center (США), в частности, выпускниками 1ЛМИ М. О. Коноплевой и С. Н. Коноплевым, привели к заключению договора о сотрудничестве между Институтом и MDACC в 2017 году. При участии ведущих экспертов данного центра в июне 2017 года в Санкт-Петербурге прошла конференция «Современные стратегии терапии и горизонты в гематологии и онкологии». Послушать и принять участие в дискуссии по разным направлениям в гематологии приехали более 300 врачей-гематологов и врачей лабораторной диагностики, а также ученые не только из России, но и из постсоветских государств (Белоруссия, Узбекистан, Казахстан, Армения). Более 20 экспертов в области гематологии и онкологии из Америки, стран Европы и из России сделали доклады о современных способах диагностики и терапии. Важную часть докладов составили презентации перспектив в лечении пациентов заболеваниями крови. Конференция стала ярким и запоминающимся мероприятием, наиболее крупным в истории Института до настоящего времени.
С 2016 года сотрудники Института и врачи-гематологи ежегодно выступают с докладами на конференции SOHO (Society of Hematologic Oncology), которая проводится под эгидой MDACC в г. Хьюстон. С 2017 года директор Института проф. А. Ю. Зарицкий имеет статус почетного посла SOHO на территории России.
С 2017 года стажировки в MDACC прошли несколько сотрудников Института, в частности Ю. В. Миролюбова. Молодой врач-гематолог Н. С. Тимофеева в настоящее время выполняет научную работу в этом центре.
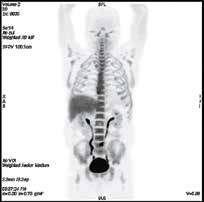
121031100301-1. «Прогнозирование эффективности специфической терапии с помощью позитронной эмиссионной томографии с 3′-дезокси-3′-[18F]фтор-л-тимидин при миелоидных новообразованиях». Выявлено, что степень захвата 18F-ФЛТ коррелирует с объемом опухолевой массы и пролиферативной активностью злокачественных гемопоэтических клеток. Так, при острых миелоидных лейкозах (ОМЛ) активный захват 18F-ФЛТ в костном мозге был выявлен в дебюте болезни, при его рецидиве или рефрактерном течении. Все параметры ПЭТ-КТ 18F-ФЛТ были сопоставлены с показателями захвата тимидина у пациента без онкологической патологии. При хронических миелоидных новообразованиях активность тимидина в костном мозге была существенно выше у пациентов с трансформацией в бластный криз. У последних этот показатель был сравним с уровнем захвата тимидина у пациентов с ОМЛ. На данном этапе продолжается анализ показателей для выявления роли исследования в оценке пролиферативной активности печени и селезенки при хронических миелоидных новообразованиях.
 |
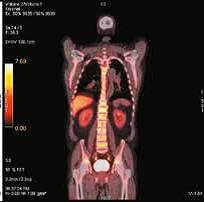 |
| ПЭТ-КТ с 18F-ФЛТ в норме с физиологическим накоплением РФП в печени и КМ | |
122041400269-9. «Разработка технологии производства и стандарта качества линейки радиофармацевтических препаратов для тераностики нейроэндокринных опухолей с целью персонализации противоопухолевого лечения». Была усовершенствована технология радио- химического синтеза радиофармацевтического препарата (РФП) — меченого агониста соматостатиновых рецепторов 68Ga-ДОТА-ТОК на оригинальном модуле синтеза DATVOS, создана стандартная операционная процедура его изготовления, разработаны методики контроля качества и создана спецификация по основным показателям: подлинность, объемная активность, радиохимическая чистота, радионуклидные примеси, химические примеси, упаковка, маркировка, хранение, исследование микробиологических характеристик. Разработанный процесс позволяет получать препарат с воспроизводимыми характеристиками, соответствующими европейской и американской фармакопеям. Полученные серии препарата были стабильны в течение 4 часов, что и определяет срок годности РФП.
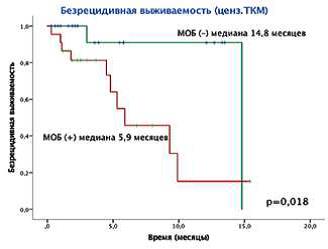
АААА-А20-120092490048-9. «Метод оценки уровня минимальной остаточной болезни (МОБ) у пациентов с впервые выявленным острым миелоидным лейкозом в постиндукционном периоде с помощью проточной цитофлуометрии». В результате проведенного исследования определена значимость достижения уровня МОБ менее 0,01 % после 1 курса терапии для прогнозирования развития раннего рецидива (в течение 6 месяцев) (61,5 % против 14,3 %, р = 0,002), снижения безрецидивной (5,9 месяца против недостижения медианы, р = 0,019) и общей (9,5 месяца против недостижения медианы, р = 0,032) выживаемости, в том числе в группах низкого и промежуточного генетического риска: медиана БРВ 6,75 месяца против недостижения медианы (р = 0,011) и медиана КЧР 5,28 месяца против недостижения медианы (р = 0,014). Применение разработанного метода прогнозирования течения заболевания и определения показаний к выполнению аллогенной ТГСК позволяет снизить частоту развития рецидива заболевания, оптимизировать программу терапии за счет сокращения количества курсов консолидации для пациентов с показаниями к алло-ТКМ и отказаться от использования высокотоксичного дорогостоящего метода лечения (ТГСК) в группе пациентов низкого и промежуточного риска с МОБ-негативным статусом после 1 курса терапии.
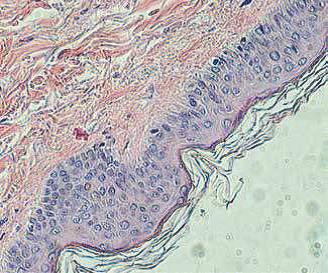
121031100307-3. «Разработка нового способа прогнозирования начала острой реакции трансплантата против хозяина и тяжести ее течения на основании динамики клеточных и гуморальных маркеров». Проведено иммуногистохимическое окрашивание биоптатов кожи у 12 пациентов, выполнен анализ образцов кала методом латеральной иммунохроматографии для определения фекального кальпротектина у 74 пациентов, исследованы уровни фекального зонулина методом иммуноферментного анализа у 75 пациентов. Проанализированы основные таргетные события у исследуемой группы. Продолжено создание банка биообразцов у пациентов после алло-ТГСК, а также биоптатов кожи при развитии клинической картины о.РТПХ с поражением кожи. Проведен анализ плазмы от 84 пациентов после алло-ТГСК в рамках оценки уровней цитокинов (IL-6, sTNFR1) и маркеров клеточного повреждения (ST2, REG3-альфа). При микроскопическом анализе выявлена повышенная экспрессия элафина (более 50 % толщины эпидермиса) в образцах кожи у пациентов с клинической картиной РТПХ кожи. По результатам исследования выявлено статистически значимое повышение уровня кальпротектина и зонулина в кале у группы пациентов с развившейся РТПХ желудочно-кишечного тракта по сравнению с пациентами без РТПХ (р = 0,05). Выявлена повышенная экспрессия элафина в образцах кожи у пациентов с клинической картиной РТПХ кожи. Проводится статистическая обработка результатов анализа уровней цитокинов в плазме.
Полученные результаты позволяют предположить, что фекальный кальпротектин и фекальный зонулин являются диагностическими маркерами развития РТПХ с поражением желудочно-кишечного тракта, а повышенная экспрессия элафина в коже — диагностическим и прогностическим маркером течения острой РТПХ с поражением кожи. Дальнейшее исследование этой темы, расширение размеров когорты позволят подтвердить выявленные закономерности и разработать диагностический протокол, направленный на раннее выявление РТПХ и прогнозирование ее течения.
2023 год
Патент 2796106 от 17.05.2023.
«Радиофармацевтический препарат для диагностики рака предстательной железы методом позитронной эмиссионной томографии и способ его получения».
Авторы: Орлова А. М., Томачев В. М., Тимофеев В. В., Рыжкова Д. В., Абузаед А.Т., Ринне С.С., Розенстрём У.Х., Лундмарк Ф.К.
2022 год
Патент 2022621999 09.08.2022.
«Регистр пациентов с врожденным гиперинсулинизмом, впервые пролеченных в Российской Федерации по новому (международному) протоколу».
Авторы: Никитина И.Л., Саракаева Л. Р., Рыжкова Д. В., Митрофанова Л. Б., Баиров В. Г., Сухоцкая А. А., Смородин А. П., Иобст О.И., Красичков А. С., Санарова К. Е.
Немаловажную часть деятельности Института составляет последипломная подготовка и стажировка врачей. В рамках этой работы оказывается консультативная и методическая помощь сотрудникам учреждений практического здравоохранения Санкт-Петербурга и других регионов Северо-Западного региона Российской Федерации путем организации и проведения семинаров, научно-практических конференций, чтения лекций для врачей по актуальным вопросам диагностики и лечения заболеваний по профилю Института.
Лекции и семинары на образовательных курсах проводятся сотрудниками института гематологии и затрагивают не только проблемы патогенеза, диагностики и лечения гематологических заболеваний, но и вопросы сопроводительной антибактериальной, противогрибковой и противовирусной, а также интенсивной терапии у данных пациентов.
В 2017 году в рамках международной программы ERSAP фонда iCMLf на базе Института прошли стажировку доктора из Киргизии и республики Белоруссия.
В декабре 2017 года на форуме iCMLf в Атланте (США) Е. Г. Ломаиа успешно выступила с докладом о результатах и перспективах сотрудничества между институтом и фондом iCMLf.
Институт сформировался и развивается как передовой гематологический, ревматологический и онкологический центр.
Работы в области миелоролиферативных заболеваний будут посвящены выявлению иммунных предикторов эффективности ИТК и роли SOCE (Store Operated Calcium Entry) в патогенезе МПЗ, а также поиску новых мишеней для разработки терапевтических подходов при МПЗ. В нашей работе мы планируем изучить иммунный профиль: экспрессию и функциональную активность субпопуляций Т-клеток, рецептора PD-1; полиморфизм генов, кодирующих другие T-клеточные рецепторы; экспрессию лигандов на поверхности лейкемических клеток. Также будет изучена экспрессия ключевых белков и функциональный статус SOCE и их влияние на функциональную и пролиферативную активность эффекторных иммунных клеток и лейкемических клеток при МПЗ, а также на клетки микроокружения. Планируется создание регистра пациентов ХМЛ с неудачей терапии ИТК, включая пациентов с прогрессией болезни в бластный криз, а также биобанкирование их образцов крови и костного мозга. Выявление новых прогностических маркеров поможет в персонализации тактики ведения пациентов, улучшит эффективность ИТК. Кроме того, при благоприятном иммунном профиле будет возможна безопасная отмена ИТК в более ранние сроки у пациентов ХМЛ с глубоким молекулярным ответом. Отмена ИТК улучшит качество жизни пациентов, а увеличение доли пациентов, в более раннем периоде прекративших терапию ИТК, снизит расходы здравоохранения на лечение больных ХМЛ. В перспективе SOCE может представлять новую терапевтическую мишень для регуляции иммунного ответа на опухолевые клетки и подавления опухолевых клеток при МПЗ. Выявление механизмов иммунного контроля может быть также основой для разработки иммуномодулирующей терапии.
С целью улучшения результатов лечения опухолей ЦНС в группах пациентов высокого риска будет разработан алгоритм персонификации терапии на основании молекулярно-генетического профиля опухолевой ткани с применением метода секвенирования нового поколения и секвенирования одиночных клеток. Задачами исследования будут являться: определение спектра патогенных вариантов при опухолях ЦНС, определение спектра мутаций гена PIK3CA при рецидивирующих и рефрактерных солидных опухолях у детей, создание базы данных по молекулярно-генетическим характеристикам опухолей ЦНС, выявление прогностически неблагоприятных альтерации с целью последующей интенсификации проводимой противоопухолевой терапии, разработка тактики таргетной терапии на основании молекулярно-генетического профиля у пациентов с опухолями ЦНС группы высокого риска, оценка эффективности комбинации метрономной химиотерапии в комбинации с таргетной терапией у детей с рецидивами/рефрактерными формами различных нозологических форм солидных опухолей, а также определение безопасности и токсичности метода. метрономной химиотерапии в комбинации с таргетной терапией
Дальнейшие работы по CAR-T терапии будут посвящены получению эффективных биспецифичных CAR-T нового поколения, распознающих лиганды NKG2D и опухоль-специфичные антигены Her2 или EGFR. Это позволит увеличить эффективность терапии и снизить вероятность рецидива в связи с потерей экспрессии антигена. Т-лимфоциты предполагается модифицировать таким образом, что они будут экспрессировать два химерных антигенных рецептора одновременно, один из которых NKG2D. Таким образом, планируется увеличить NKGD2 эффективность генетической конструкции, не усиливая токсичность за счет специфичности второго антигена. Будут также проведены доклинические исследования CAR-T на базе SPF-вивария ФГБУ «НМИЦ им. В.А. Алмазова». Кроме того, планируется сравнительный анализ сразу четырех вариантов anti-BCMA CAR-T: BCMA-28-CD3, BCMA-41BBCD3, BCMA-GITR-CD3, BCMA-ICOS-CD3 и определить наиболее оптимальный вариант для терапии множественной миеломы.
Острые миелобластные лейкозы.
На протяжении 2022 года продолжалась работа по изучению ОМЛ, сосредоточенная на наиболее актуальных направлениях, включающих анализ генетической гетерогенности заболевания, прогностической значимости уровня минимальной остаточной болезни, эффективности включения новых таргетных препаратов в программы терапии пациентов с ОМЛ, а также изучение редких, прогностически неблагоприятных вариантов ОМЛ с экстрамедуллярным поражением и миелоидной саркомы. C целью детекции мутаций в генах IDH1 R132 и IDH2 R140 внедрена методика цифровой капельной ПЦР (droplet digital Polymerase Chain Reaction, ddPCR). В течение 2021 года проводился анализ полученных лабораторных и клинических данных. Выявлено пре- имущество в общей выживаемости в группе пациентов с мутированным статусом IDH1/2 (р = 0,023). Пациенты с мутациями IDH1/2 чаще достигали полной ремиссии (р = 0,043) и имели сниженный риск развития раннего (< 12 мес.) рецидива (р = 0,041). Пациенты с нормальным кариотипом и диким типом DNMT3A имели лучшие показатели общей выживаемости (ОВ) по сравнению с пациентами с мутацией гена DNMT3A (p = 0,012).
Разработка методики оценки МОБ методом проточной цитофлуометрии может стать основой персонифицированного подхода к определению группы риска и основанием для выбора метода лечения, оптимального для каждого конкретного пациента. В рамках дальнейшего развития направления персонификации терапии ОМЛ проводится изучение оценки методом количественной ПЦР высокоспецифичных молекулярных маркеров (RUNX1-RUNX1T1, CBF-MYH11, мутации NPM1) в постиндукционном периоде и корреляция значений с результатами лечения.
BTK and PLCG2 remain unmutated in one third of patients with CLL relapsing on ibrutinib. Silvia Bonfiglio, Lesley-Ann Sutton, Viktor Ljungström, Antonella Capasso, Tatjana Pandzic, Simone Weström, Hassan Foroughi-Asl, Aron Skaftason, Anna Gellerbring, Anna Lyander, Francesca Gandini, Gianluca Gaidano, Livio Trentin, Lisa Bonello, Gianluigi Reda, Csaba Bödör, Niki Stavroyianni, Constantine S. Tam, Roberto Marasca, Francesco Forconi, Panayiotis Panayiotidis, Ingo Ringshausen, Ozren Jaksic, Anna Maria Frustaci, Sunil Iyengar, Marta Coscia, Stephen P. Mulligan, Loïc Ysebaert, Vladimir Strugov, Carolina Pavlovsky, Renata Walewska, Anders Österborg, Diego Cortese, Pamela Ranghetti, Panagiotis Baliakas, Kostas Stamatopoulos, Lydia Scarfò, Richard Rosenquist, Paolo Ghia. Blood advances. 2023. Vol. 7, № 12. P. 2794—2806. DOI: 10.1182/bloodadvances.2022008821. Scopus Q1/Q2. IF 7,642
Potential Binding Sites of Pharmacological Chaperone NCGC00241607 on Mutant β-Glucocerebrosidase and Its Efficacy on Patient-Derived Cell Cultures in Gaucher and Parkinson's Disease. Alena E. Kopytova, George N. Rychkov, Alexander A. Cheblokov, Elena V. Grigor’eva, Mikhail A. Nikolaev, Elena S. Yarkova, Diana A. Sorogina, Farid M. Ibatullin, Galina V. Baydakova, Artem D. Izyumchenko, Daria A. Bogdanova, Vitali M. Boitsov, Akim V. Rybakov, Irina V. Miliukhina, Vadim A. Bezrukikh, Galina N. Salogub, Ekaterina Y. Zakharova, Sofya N. Pchelina, Anton K. Emelyanov. International Journal of Molecular Sciences. 2023. Vol. 24, № 10. 9105. DOI: 10.3390/ijms24109105. Scopus Q1/Q2. IF 6,208
Evaluation of CAR-T Cells' Cytotoxicity against Modified Solid Tumor Cell Lines. Aigul Kh. Valiullina, Ekaterina A. Zmievskaya, Irina A. Ganeeva, Margarita N. Zhuravleva, Ekaterina E. Garanina, Albert A. Rizvanov, Alexey V. Petukhov, Emil R. Bulatov. Biomedicines. 2023. Vol. 11, № 2. 626.DOI: 10.3390/biomedicines11020626. Scopus Q1/Q2. IF 4,651
Сytotoxic effect of CAR-T cells against modified MCF-7 breast cancer cell line. Aigul Kh. Valiullina, Ekaterina A. Zmievskaya, Irina A. Ganeeva, Margarita N. Zhuravleva, Ekaterina E. Garanina, Albert A. Rizvanov, Alexey V. Petukhov, Emil R. Bulatov. Molecular Biology Research Communications. 2023. Vol. 12, № 4. P. 139-148. DOI: 10.22099/mbrc.2023.47125.1820. Scopus Q3/Q4. IF 2,022
Прогностическое значение соматических мутаций в генах эпигенетической регуляции при острых миелоидных лейкозах в реальной клинической практике: результаты наблюдательного неинтервенционного проспективного межрегионального исследования. А.А. Шатилова, И.Г. Будаева, А.В. Петухов, С.А. Силонов, А.Е. Ершова, Т.С. Никулина, Ю.Д. Матвиенко, Ю.В. Миролюбова, К.В. Богданов, Л.В. Анчукова, Ю.С. Нередько, С.Ю. Тяско, О.Е. Очирова, А.Г. Карпова, Э.Р. Васильева, О.Д. Сердюк, Д.А. Яскульский, Д.В. Букин, Ю.А. Алексеева, Е.Г. Ломаиа, Л.Л. Гиршова. Клиническая онкогематология. Фундаментальные исследования и клиническая практика. 2023. Т. 16, № 2. С. 174-185. DOI: 10.21320/2500—2139-2023-16-2-174-185. Scopus Q3/Q4. IF 0,67
Классические и активирующие химерные антигенные рецепторы PD-1 как элемент мультитаргетного подхода в лечении гематологических и солидных новообразований. Левчук Ксения Александровна, Голдаева А.А., Столярова Е.А., Матейкович П.А., Валиуллина А.Х., Булатов Э.Р., Петухов А.В., Дакс А.А., Барлев Н.А., Байдюк Е.В., Торопова Я.Г. Клиническая онкогематология. Фундаментальные исследования и клиническая практика. 2023. Т. 16, № 3. С. 268-279. DOI: 10.21320/2500—2139-2023-16-3-268-279. Scopus Q3/Q4. IF 0,67
Multicenter non-interventional retrospective study: prevalence, clinical characteristics and approaches to the treatment of acute and chronic graft-versus-host disease in the Russian Federation. Moiseev Ivan S., Drokov Mikhail Yu., Motorin Dmitry V., Badaev Renat S., Petrova Galina D., Bykova Tatyana A., Beynarovich Anastasia V., Kuzmina Larisa A., Dovydenko Maria V., Vasil'eva Vera A., Reshetova Anastasia I., Nikiforova Natalya M., Zubarovskaya Ludmila S., Kulagin Alexander D., Parovichnikova Elena N. Cellular Therapy and Transplantation. 2023. Т. 12, № 4. С. 11-23. DOI: 10.18620/ctt-1866—8836-2023-12-4-11-23. Scopus Q3/Q4. IF 0,563
Graft preservation in haploidentical hematopoietic stem cell transplantation with post-transplant cyclophosphamide: single center experience. Badaev Renat S., Zammoeva Darina B., Chistyakov Vasiliy S., Pestakov Alexander Yu., Girshova Larisa L., Budaeva Irina G., Siordiya Nadiya T., Alekseeva Yuliya A., Lomaia Elza G., Zaritskey Andrey Yu., Motorin Dmitriy V. Cellular Therapy and Transplantation. 2023. Т. 12, № 4. С. 31-37. DOI: 10.18620/ctt-1866—8836-2023-12-4-31-37. Scopus Q3/Q4. IF 0,563
2023 год
Погосян К.А., Каронова Т.Л., Рыжкова Д.В., Яневская Л.Г., Цой У.А., Юдина О.В., Иваниха Е.В., Гринева Е.Н. Возможности ПЭТ/КТ с 11С-холином как метода топической диагностики аденом околощитовидных желез у больных первичным гиперпаратиреозом. Трансляционная медицина. 2023; 10 (2): 88-95. DOI:10.18705/2311—4495-2023-10-2-88-95. IF 0,864.
Майрина С. В., Рыжкова Д. В., Митрофанова Л. Б., Рыжков А. В., Муртазалиева П. М., Моисеева О. М. Современные подходы к диагностике и лечению саркоидоза сердца: результаты когортного исследования. Российский кардиологический журнал. 2023; 28 (5): 23-30. DOI:10.15829/1560—4071-2023-5301. IF 2,437.
Fanny Lundmark, Ayman Abouzayed, Sara S. Rinne, Vasiliy Timofeev, Nadezhda Sipkina, Maria Naan, Anastasia Kirichenko, Maria Vasyutina, Daria Ryzhkova, Vladimir Tolmachev, Ulrika Rosenström, Anna Orlova. Preclinical Characterisation of PSMA/GRPR-Targeting Heterodimer [68Ga]Ga-BQ7812 for PET Diagnostic Imaging of Prostate Cancer: A Step towards Clinical Translation. Cancers. 2023; 15 (442): 1-15. DOI:10.3390/cancers15020442. IF 6,575.
Silvia Bonfiglio, Lesley-Ann Sutton, Viktor Ljungström, Antonella Capasso, Tatjana Pandzic, Simone Weström, Hassan Foroughi-Asl, Aron Skaftason, Anna Gellerbring, Anna Lyander, Francesca Gandini, Gianluca Gaidano, Livio Trentin, Lisa Bonello, Gianluigi Reda, Csaba Bödör, Niki Stavroyianni, Constantine S. Tam, Roberto Marasca, Francesco Forconi, Panayiotis Panayiotidis, Ingo Ringshausen, Ozren Jaksic, Anna Maria Frustaci, Sunil Iyengar, Marta Coscia, Stephen P. Mulligan, Loïc Ysebaert, Vladimir Strugov, Carolina Pavlovsky, Renata Walewska, Anders Österborg, Diego Cortese, Pamela Ranghetti, Panagiotis Baliakas, Kostas Stamatopoulos, Lydia Scarfò, Richard Rosenquist, Paolo Ghia. BTK and PLCG2 remain unmutated in one third of patients with CLL relapsing on ibrutinib. Blood advances. 2023; 1-35. DOI:10.1182/bloodadvances.2022008821. IF 7,642.
Саракаева Л.Р., Рыжкова Д.В., Митрофанова Л.Б., Баиров В.Г., Сухоцкая А.А., Смородин А.П., Ефтич Е.А., Кельмансон И.А., Никитина И.Л. Параметры электроэнцефалограммы у детей с врожденным гиперинсулинизмом, пролеченных по международному протоколу. Проблемы эндокринологии. 2023; 69 (1): 68-75. DOI:10.14341/probl13174. IF 1,123.
Aigul Kh. Valiullina, Ekaterina A. Zmievskaya, Irina A. Ganeeva, Margarita N. Zhuravleva, Ekaterina E. Garanina, Albert A. Rizvanov, Alexey V. Petukhov, Emil R. Bulatov. Evaluation of CAR-T Cells' Cytotoxicity against Modified Solid Tumor Cell Lines. Biomedicines. 2023; 11 (2): 626 1-22. DOI:10.3390/biomedicines11020626. IF 4,651.
Karina Pogosian, Tatiana Karonova, Daria Ryzhkova, Liubov Yanevskaya, Uliana Tsoy, Olga Yudina, Gleb Berkovich, Anna Dalmatova, Elena Grineva. 11C-methionine PET/CT and conventional imaging techniques in the diagnosis of primary hyperparathyroidism. Quantitative Imaging in Medicine and Surgery. 2023; 13 (4): 1-7. DOI:10.21037/qims-22-584. IF 4,63.
2022 год
Murtazalieva Patimat, Ryzhkova Darya, Malev Eduard, Zhiduleva Ekaterina, Moiseeva Olga Prediction of aortic stenosis progression by 18F-FDG and 18F-NaF PET/CT in different aortic valve phenotypes Frontiers in Pharmacology 2022; 13: 909975 1-11 DOI:10.3389/fphar.2022.909975 6,6
Aleksei Titov, Yaroslav Kaminskiy, Irina Ganeeva, Ekaterina Zmievskaya, Aygul Valiullina, Aygul Rakhmatullina, Alexey Petukhov, Regina Miftakhova, Albert Rizvanov, Emil Bulatov Knowns and Unknowns about CAR-T Cell Dysfunction Cancers 2022; 14 (4): 1078 1-24 DOI:10.3390/cancers14041078 6,575
Olga Fedorova, Alexandra Daks, Sergey Parfenyev, Oleg Shuvalov, Sofia Netsvetay, Julia Vasileva, Anastasia Gudovich, Vasilii Golotin, Oleg Semenov, Alexey Petukhov, Ekaterina Baiduik, Nurken Berdigaliyev, Eugene M. Tulchinsky, Nikolai A. Barlev Zeb1-mediated autophagy enhances resistance of breast cancer cells to genotoxic drugs Biochemical and Biophysical Research Communications 2022; 589: 29-34 DOI:10.1016/j.bbrc.2021.11.088 6,5
Alexander V. Fonin, Sergey A. Silonov, Anna S. Fefilova, Olesya V. Stepanenko, Anastasia A. Gavrilova, Alexey V. Petukhov, Anna E. Romanovich, Anna L. Modina, Tatiana S. Zueva, Evgeniy M. Nedelyaev, Nadejda M. Pleskach, Mirya L. Kuranova, Irina M. Kuznetsova, Vladimir N. Uversky, Konstantin K. Turoverov. New Evidence of the Importance of Weak Interactions in the Formation of PML-Bodies International Journal of Molecular Sciences 2022; 23 (3): 1613 1-13 DOI:10.3390/ijms23031613 6,208
Daria Ryzhkova, Lubov Mitrofanova, Uliana Tsoy, Elena Grineva, Evgeny Schlyakhto Dual-tracer PET/CT imaging to determine tumor heterogeneity in a patient with metastatic ACTH-secreting neuroendocrine neoplasm: A case report and literature review Frontiers in Endocrinology 2022; 1-8 DOI:10.3389/fendo.2022.958442 6,055
Morgacheva D, Daks A, Smirnova A, Kim A, Ryzhkova D, Mitrofanova L, Staliarova A, Omelina E, Pindyurin A, Fedorova O, Shuvalov O, Petukhov A, Dinikina Y Case Report: Primary Leptomeningeal Medulloblastoma in a Child: Clinical Case Report and Literature Review Frontiers in Pediatrics 2022; 1-7 DOI:10.3389/fped.2022.925340 3,569
Sergey V. Nesterov, Emmanuel Deshayes, Luis Eduardo Juarez-Orozco, Robert A. deKemp, Roberto Sciagrà, Simona Malaspina, Leonardo Settimo, Chunlei Han, Darja V. Ryzhkova, Irina S. Kostina, Kilem L. Gwet, John O. Prior, Juhani M. Knuuti Myocardial perfusion quantification with Rb-82 PET: good interobserver agreement of Carimas software on global, regional, and segmental levels Annals of Nuclear Medicine 2022; 1-8 DOI:10.1007/s12149-022-01729-5 2,668
2021 год
Uyanik B, Goloudina AR, Akbarali A, et al. Inhibition of the DNA damage response phosphatase PPM1D reprograms neutrophils to enhance anti-tumor immune responses. Nat Commun. 2021;12 (1):3622. Published 2021 Jun 15. doi:10.1038/s41467-021-23330-6. IF 13.783. Режим доступа: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8206133/
Daks A, Petukhov A, Fedorova O, et al. The RNA-binding protein HuR is a novel target of Pirh2 E3 ubiquitin ligase. Cell Death Dis. 2021;12 (6):581. Published 2021 Jun 5. doi:10.1038/s41419-021-03871-w. IF 7.568. Режим доступа: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8179929/
Passamonti F, Gupta V, Martino B, et al. Comparing the safety and efficacy of ruxolitinib in patients with Dynamic International Prognostic Scoring System low- , intermediate-1- , intermediate-2- , and high-risk myelofibrosis in JUMP, a Phase 3b, expanded-access study. Hematol Oncol. 2021;39 (4):558-566. doi:10.1002/hon.2898. IF 2.615. Режим доступа: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8518822/
Bogdanov KV, Merzlikina OV, Mirolyubova YV, Girshova LL, Lomaia EG, Zaritskey AY. [CASC5 Gene Expression Changes Correlate with Targeted Mutations in Leukemia]. Mol Biol (Mosk). 2021;55 (1):139-151. doi:10.31857/S002689842101002X. IF 2.035. Режим доступа: https://pubmed.ncbi.nlm.nih.gov/33566033/
2020 год
Shuvalov O, Kizenko A, Petukhov A, et al. SEMG1/2 augment energy metabolism of tumor cells. Cell Death Dis. 2020;11 (12):1047. Published 2020 Dec 11. doi:10.1038/s41419-020-03251-w. IF 7.568. Режим доступа: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7733513/
H. Lipton, F. X. Mahon, J. Mayer, F. Nicolini, D. Niederwieser, F. Pane, J. P. Radich, D. Rea, J. Richter, G. Rosti,P. Rousselot, G. Saglio, S. Saußele, S. Soverini, J. L. Steegmann, A. Turkina, A. Zaritskey et al. European LeukemiaNet 2020 recommendations for treating chronic myeloid leukemia. Leukemia. 2020;34:966–984. IF 8,70. Режим доступа: https://www.nature.com/articles/s41375-020-0776-2.
Heibl S., Hehlmann R., Faber E.N., Turkina A.G., Ossenkoppele G., Höglund M., Zaritsky A.Yu., Griskevicius L., Olsson-Strömberg U., Everaus H., Koskenvesa P., Labar B., Sacha T. et al. The EUTOS long-term survival (ELTS) score is superior to the Sokal score for predicting survival in chronic myeloid leukemia. Leukemia. 2020;34 (8):2138—2149. IF 8,70. Режим доступа: https://pubmed.ncbi.nlm.nih.gov/32601376/.
Blonde L., Belousova L., Fainberg U., Garcia-Hernandez P.A., Jain S.M., Kaltoft M.S., Mosenzon O., Nafach J., Palle M.S., Rea R. Liraglutide as add-on to sodium-glucose co-transporter-2 inhibitors in patients with inadequately controlled type 2 diabetes: LIRA-ADD2SGLT2i, a 26-week, randomized, double-blind, placebo-controlled trial. DIABETES OBESITY & METABOLISM. 2020; 22 (6):929-937. IF 6,10. Режим доступа: https://pubmed.ncbi.nlm.nih.gov/31984646/.
Bosch F., Cantin G., Cortelezzi A., Knauf W., Tiab M., Turgut M., Zaritsky A.Yu., Merot J.L., Tausch E., Stilgenbauer S., Trunzer K., Robson S., Gresko E., Böttcher S., Foà R., Leblond V. Obinutuzumab plus fludarabine and cyclophosphamide in previously untreated, fit patients with chronic lymphocytic leukemia: a subgroup analysis of the green study. 2020; 34 (2): 441-450. IF 8,70. Режим доступа: https://www.nature.com/articles/s41375-019-0554-1.
Yassin M., Pocali B., Barna G., Chiarenza A., Dos Santos G., Nikitin E., Andres M., Dimou M., Doubek M., Enrico A., Hakobyan Y., Kalashnikova O., Ortiz Pareja M., Papaioannou M., Rossi D., Shah N., Shrestha A. et al. COVID-19 severity and mortality in patients with chronic lymphocytic leukemia: a joint study by ERIC, the European Research Initiative on CLL, and CLL Campus. Leukemia. 2020;34 (9): 2354—2363. IF 8,70. Режим доступа: https://www.nature.com/articles/s41375-020-0959-x.
2023 год
Быкова К.М., Кашерининов И.Ю., Рутковский Р.В., Рыжкова Д.В., Саввина И. А. Возможности ПЭТ/КТ С 18F-фтордезоксиглюкозой в диагностике сепсис-ассоциированной энцефалопатии // Российский нейрохирургический журнал имени проф. А.Л. Поленова. Том XV. Спецвыпуск. Сборник материалов XXII всероссийской научно-практической конференции «Поленовские чтения». 2023. — с.2.
2022 год
Алексеева Т.М., Андреева А.А., Ефимцев А.Ю., Гринева А.А., Железникова Г.Ф., Золотова М.А., Ибрагимова О.М., Иванов В.В., Иванов Д.О., Иванова Г.П., Иванова М.В., Иванова Р.А., Мария Александровна, Строкова Т.В., Суспицын Е.Н., Тебеньков А.В., Терновых И.К., Титова М.А., Тихомиров Д.С., Тихомирова К. К., Топузова М.П., Тян Н. С., Улитин А.Ю., Рыжкова Д.В., Чухловина М. Л., Чайковская А.Д, Шарипова Е. В., Шестов А.В., Шилова И. В., Шляхто Е.В., Юркина Е. А., Яровая Ю. А., Яковлева Т.В. «Старые» и «новые» инфекции у детей: трудные случаи. ООО «АЛЬГИЗ». 2022.
Ломаиа Елза Галактионовна, ведущий научный сотрудник отдела клинической онкогематологии
E-mail: lomaia_eg@almazovcentre.ru