Разработка новых технологий профилактики и лечения сердечной недостаточности на основе нейромодуляции
Крупный научный проект при поддержке Министерства науки и высшего образования (соглашение № 075-15-2020-800)
I. Информация на первой странице проекта
Крупный научный проект, состоящий из нескольких ключевых направлений, получил поддержку Министерства науки и высшего образования на 2020—2022 гг. В рамках проекта будет разработана концепция комплексного воздействия на автономную нервную систему для коррекции и профилактики хронической сердечной недостаточности при сердечно-сосудистой патологии.
Мультидисциплинарные работы проводятся по следующим направлениям:
- Раздел «ишемия миокарда»: в этот раздел войдут исследования применения адипокинов для протекции миокарда и электрическая активация блуждающего нерва при ишемии и реперфузии; математическое моделирование влияния гуморальных факторов на функцию миокарда в условиях ишемии.
- Раздел «автономная регуляция в аритмогенезе»: в этом разделе запланированы исследования по нейрогенным механизмам индукции и поддержания фибрилляции предсердий и разработке новых методов лечения фибрилляции предсердий.
- Раздел «автономная регуляция кровообращения при системной и легочной гипертензии и хронической сердечной недостаточности»: будут проведены исследования влияния вегетативной нервной системы на ремоделирование малого круга кровообращения при легочной гипертензии; будет проводиться разработка подходов к неинвазивной стимуляции спинного мозга при гипотензии; новые методы коррекции легочной гипертензии, включая денервацию легочной артерии; вегетативная регуляция после трансплантации сердца.
- Раздел «профилактика и лечение сердечной недостаточности»: в основном, клинический проект, в котором изучается вклад автономной дисфункции в патогенез развития и прогрессирования сердечной недостаточности; роль циркулирующих биомаркеров и тестов автономной регуляции в прогнозировании исходов сердечно-сосудистой патологии.
В реализации крупного проекта будут принимать сотрудники экспериментальных и клинических подразделений Центра Алмазова, часть работ будет осуществляться в сотрудничестве с учеными из других учреждений: Уральский Институт иммунологии и физиологии (Екатеринбург), Гентский Университет (Гент, Бельгия), Университет ИТМО (Санкт-Петербург), Балтийский Государственный технический университет ВОЕНМЕХ им. Д.Ф. Устинова (Санкт-Петербург), НИИ физиологии им. И.П. Павлова (Санкт-Петербург).
Ожидается, что результаты исследований дадут толчок развитию направления нейромодуляции в лечении сердечно-сосудистых заболеваний на мировом уровне. Среди критериев успешности реализации грантового проекта – беспрецедентное привлечение молодых ученых, публикации в высокорейтинговых журналах, международное сотрудничество.
II. Разделы сайта
- О проекте
- Цели и задачи
- Структура работы над проектом
- Экспертный совет
- Контакты
- Исследования
- Адипокины и подпороговая активация блуждающего нерва при ишемическом и реперфузионном повреждении.
- Математическое моделирование влияния адипокинов на функцию сердца при ишемии/реперфузии.
- Адренергическая и холинергическая активность в патогенезе фибрилляции предсердий, химическая модуляция автономной нервной регуляции.
- Вегетативная нервная система при правожелудочковой недостаточности и легочной гипертензии.
- Коррекция ортостатической и медикаментозной гипотензии путем электрической стимуляции спинного мозга.
- Фиброоптическая денервация сосудов при сердечно-сосудистой патологии и сердечной недостаточности.
- Адаптированная денервация легочной артерии для коррекции легочной гипертензии.
- Автономная дисфункция при реабилитации после трансплантации сердца.
- Дисфункция автономной нервной системы и биомаркеры в патогенезе, прогрессировании и прогнозировании исходов при сердечной недостаточности.
- Новости
- Научные публикации
III. Цели и задачи
Цель:
Изучить фундаментальные механизмы участия автономной нервной системы в патогенезе заболеваний системы кровообращения и разработать новые технологии лечения cердечной недостаточности на основе нейромодуляции.
Задачи:
- Изучить эффекты адипокинов и электрической подпороговой активации блуждающего нерва на миокард и проводящую систему сердца при ишемическом и реперфузионном повреждении.
- Провести математическое моделирование влияния адипокинов на функцию сердца человека в условиях ишемии/реперфузии на основе полученных экспериментальных данных.
- Изучить фундаментальные механизмы инициации и поддержания фибрилляции предсердий, связанные со сравнительным вкладом повышения активности адренергических и холинергических нейронов, входящих в состав ганглионарных сплетений сердца, а также экспериментально обосновать методику химической аблации ганглионарных сплетений.
- Изучить влияние вегетативной нервной системы на процессы ремоделирования сосудов малого круга кровообращения и правого желудочка при легочной артериальной гипертензии и хронической тромбоэмболической легочной гипертензии.
- Разработать методические основы и оценить эффективность применения чрескожной электрической стимуляции спинного мозга для коррекции артериальной гипотензии при ортостазе, а также у пациентов с артериальной гипотензией на фоне сердечной недостаточности.
- Разработать подходы к фиброоптической лазерной деструкции нервов и нервных ганглиев для транссосудистой денервации при сердечно-сосудистой патологии, ассоциированной с развитием и прогрессированием хронической сердечной недостаточности.
- Разработать подход к адаптированной и персистирующей денервации легочной артерии с использованием стимуляционного картирования как метода лечения легочной гипертензии.
- Определить взаимосвязь восстановления автономного контроля кровообращения и регресса сердечной недостаточности с целью оптимизации процесса реабилитации после трансплантации сердца на экспериментальной модели и у пациентов с терминальной хронической сердечной недостаточностью.
- Изучить вклад дисфункции автономной нервной системы и циркулирующих биомаркеров в патогенез, прогрессирование и прогнозирование исходов сердечно-сосудистой патологии и сердечной недостаточности в клинических условиях.
IV. Структура работы над проектом
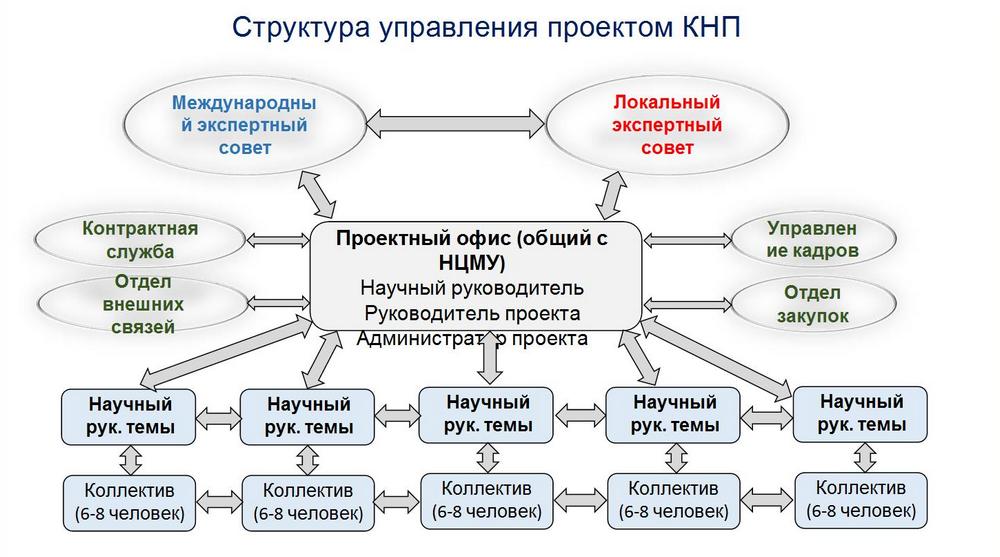
V. Экспертный совет
Экспертный совет проекта КНП
Председатель: Шляхто Е.В.
Международный консультативный совет:
Stefan Anker, Berlin, Germany
Felix Mahfoud, Homburg, Germany
Andrew Coats, UK (ESC HFA president 20-22)
Раздел «ишемия и реперфузия миокарда»
Проекты: адипокины при ишемии и реперфузии, нейростимуляция и активация блуждающего нерва при ишемии и реперфузии, математическое моделирование влияния гуморальных факторов на функцию миокарда в условиях ишемии.
| ФИО | Город, учреждение |
| Felix Mahfoud | Homburg, Saarland University, Германия |
| Jarle Vaage | Осло, Норвегия, Университет Осло |
| Mark Chapleau | Iowa University, USA |
| Tamas Szili-Torok | Роттердам, Нидерланды, Erasmus Medical Center |
| Виллевальде Светлана Вадимовна | СПб, Центр Алмазова |
| Власов Тимур Дмитриевич | СПб, ПСПбГМУ им Павлова |
| Галагудза Михаил Михайлович | СПб, Центр Алмазова |
| Козлова Светлана Николаевна | СПб, Центр Алмазова |
| Конради Александра Олеговна | СПб, Центр Алмазова |
| Костарева Анна Александровна | СПб, Центр Алмазова |
| Лебедев Дмитрий Сергеевич | СПб, Центр Алмазова |
| Митрофанова Любовь Борисовна | СПб, Центр Алмазова |
| Михайлов Евгений Николаевич | СПб, Центр Алмазова |
| Моисеева Ольга Михайловна | СПб, Центр Алмазова |
| Мошонкина Татьяна Ромульевна | СПб, Институт физиологии им. И.П. Павлова |
| Панфилов Александр Викторович | Гент, Университет Гент, Бельгия |
| Ротарь Оксана Петровна | СПб, Центр Алмазова |
| Самочерных Константин Александрович | СПб, НИИ Поленова, Центр Алмазова |
| Ситникова Мария Юрьевна | СПб, Центр Алмазова |
| Соловьева Ольга Эдуардовна | Екатеринбург, Институт иммунологии и физиологии |
| Федотов Петр Алексеевич | СПб, ПСПбГМУ им. Павлова |
| Яковлев Алексей Николаевич | СПб, Центр Алмазова |
VI. Контакты
Руководитель проекта:
Директор института экспериментальной медицины, д.м.н., проф. чл. -корр РАН Галагудза Михаил Михайлович
galagudza_mm@almazovcentre.ru
Менеджер проекта:
Заместитель директора Инстистута сердца и сосудов по научной работе, руководитель НИЛ нейромодуляции, д.м.н.
Михайлов Евгений Николаевич
e.mikhaylov@almazovcentre.ru
Администратор проекта:
Младший научный сотрудник НИЛ нейромодуляции
Вахрушев Александр Дмитриевич
vakhrushev_ad@almazovcentre.ru
VII. Исследования
Научный руководитель: д.м.н., проф., чл. -корр. РАН Галагудза Михаил Михайлович
Ответственный исполнитель: к.м.н. Полякова Екатерина Анатольевна
Состояние вопроса: Поиск подходов эффективного лечения инфаркта миокарда у миллионов людей продолжается, новые способы должны уменьшить повреждение миокарда путем модификации нейрогуморальных факторов. Научные подходы: оценка инфаркт-лимитирующего эффекта стимуляции n. vagus и адипокинов (модель in vivo и перфузия по Лангендорфу); экспрессии генов, уровней адипокинов в миокарде и сыворотке крови (методами ПЦР и ИФА); внутриклеточных киназ адипокинов в кардиомиоцитах (вестерн блот); митохондриальной дисфункции. Популяционное моделирование. Ожидаемые результаты 2020: адипокины и парасимпатическая активация при ишемии/реперфузии миокарда в эксперименте. Кардиомиоциты in vitro: анализ влияния адипокинов на электрофизиологическую и механическую активность и ремоделирование. 2021: молекулярно-генетические исследования и анализ данных. In vitro оценка электромеханической активности кардиомиоцитов. Разработка клеточных моделей. 2022: закономерности влияния адипокинов и парасимпатической стимуляции на степени ишемического повреждения.
Научный руководитель: д.м.н., проф., Соловьева Ольга Эдуардовна
Ответственный исполнитель: к.м.н. Полякова Екатерина Анатольевна
Состояние вопроса: Изучение влияния жировой ткани на электрофизиологическую функцию миокарда в рамках математических моделей проводится единственной в мире группой A. Panfilov. Научные подходы: Моделирование распространения возбуждения в миокарде с использованием монодоменной модели миокардиальной ткани; моделирования текстур тканей предсердий и желудочков; моделирование анатомических персонифицированных 3D моделей сердец пациентов для in silico исследований последствий эпикардиального ожирения при инфаркте. Перенос данных на модели сердца человека с применением нейронных сетей. Ожидаемые результаты 2020: 3D моделирование повреждения сердец крыс. 2021: 3D геометрия повреждений в сердце крыс и человека. Разработка алгоритмов генерации анатомических моделей сердца человека для проведения симуляции активации миокарда in silico. 2022: данные об эффекте применения адипокинов и вегетативной стимуляции на размер инфаркта, перенос данных на модели сердца человека.
Научный руководитель: к.б.н. Королев Дмитрий Владимирович
Ответственный исполнитель: к.м.н. Сонин Дмитрий Леонидович
Состояние вопроса: Повышение нейрональной активности ганглионарных сплетений (ГС) сердца способствует инициации и поддержанию фибрилляции предсердий. Используемые методы аблации ГС основаны на необратимом и неселективном воздействии на различные нейроны ГС, что снижает клиническую значимость процедуры. Механизм положительного влияния аблации ГС на течение ФП неизвестен. Научные подходы: Будут выполнены эксперименты на свиньях с электрофизиологическим, морфометрическим и молекулярно-биологическим исследованием. Для выключения эффекта симпатических и парасимпатических влияний со стороны ГС планируется применить селективные нейротоксины, упакованные в липосомы. Ожидаемые результаты 2020: научные данные о методике синтеза липосом и технологии инкапсулирования нейромодуляторов 6-гидроксидофамина и AF64A (этилхолина азиридина). 2021: валидация модели ФП, данные об оптимальной дозировке инкапсулированных в липосомы нейромодуляторов. 2022: данные о выраженности гистологических изменений в ГС, результаты оценки уровня экспрессии фактора роста нервов и c-Fos в ткани ГС.
Научный руководитель: д.м.н., Моисеева Ольга Михайловна
Ответственный исполнитель: к.м.н. Карпов Андрей Александрович
Состояние вопроса: Известны положительные результаты блокирования симпатических и активации парасимпатических влияний на ремоделирование правого желудочка и сосудов малого круга кровообращения (МКК) при патологии, но механизм неизвестен. Также неизвестно участие ВНС в трансформации острой ТЭЛА в ХТЭЛГ. Научные подходы: Эксперименты на монокроталиновой модели ЛАГ и эмболической модели ХТЭЛГ у крыс с нейромодуляцией с помощью вагусной денервации и блокады звездчатого ганглия. Оценка вариабельности сердечного ритма, толерантности к нагрузке, ЭХОКГ, гемодинамики, морфометрия и анализ экспрессии генетических биомаркеров. Ожидаемые результаты 2020: выявление особенностей экспрессии генов, ответственных за фиброз, в ткани легкого и ПЖ в моделях ЛАГ и ХТЭЛГ по сравнению с контролем. 2021: данные о влиянии подавления парасимпатической нервной системы на центральную гемодинамику и процессы ремоделирования ПЖ и сосудов МКК при формировании ХТЭЛГ путем 2020—1902-01-0593 25.05.2020 19:16 7 1ec81aa0fc2a6d747160e4d1b335eb8c вагусной денервации. 2022: данные о роли симпатической нервной системы в ремоделировании ПЖ и сосудов МКК на модели ЛАГ путем фармакологической блокады звездчатого ганглия.
Научный руководитель: д.м.н., Михайлов Евгений Николаевич
Состояние вопроса: Электрическая активация спинного мозга влияет на вегетативную нервную деятельность и регуляцию внутренних органов. Неинвазивная чрескожная ССМ (НЧ-ССМ) на уровне Т1-Т7 приводит к повышению артериального давления (АД) в положении лежа и стоя. Научные подходы: Будет проведена серия тестов с пассивным ортостазом у лиц с ортостатической гипотензией (инвазивная регистрация артериального давления). Высокочастотная НЧ-ССМ во время пробы будет проводиться в соответствии с ранее разработанным алгоритмом на уровнях Т1, Т5-Т8; будет выработан наиболее эффективный алгоритм стимуляции. Воспроизводимость результата будет оценена при повторных тестах. Будет создана база для разработки носимого устройства коррекции гипотензии. Новизна. Будет разработан подход к коррекции ортостатической гипотензии, в том числе при сердечной недостаточности, путем НЧ-ССМ. Сейчас не существует методов лечения этого состояния. Ожидаемые результаты 2020: проведение тестов стимуляции в различных режимах и комбинациях в пассивном ортостазе. 2021: проведение повторных тестов с разработанным алгоритмом, оценка воспроизводимости результата. 2022: модификация методики и модернизация оборудования для проведения стимуляции в амбулаторных условиях. Техническое задание для носимого прибора.
Научный руководитель: д.м.н., проф. РАН, Лебедев Дмитрий Сергеевич
Ответственный исполнитель: Вахрушев Александр Дмитриевич
Состояние вопроса: Оптоволоконные лазерные устройства используются для медицинских вмешательств. Перспективно применение лазера для денервации сосудов, ожидаются преимущества лазерной перед общепринятыми технологиями: фокусирование или коллимирование луча; адаптация глубины повреждения; сохранение эндотелия. Научные подходы: В экспериментах на свиньях и овцах будут изучены возможности и эффекты лазерной денервации легочной артерии, почечных артерий, аблации ганглионарных сплетений левого и правого предсердий. Планируется три этапа: изучение лазерного повреждения на изолированной ткани, у здоровых животных и у животных с моделированной патологией: легочная гипертензия, артериальная гипертензия, фибрилляция предсердий. Новизна. Разработка подходов к фиброоптической лазерной денервации легочной артерии, почечных артерий, левого и правого предсердий для лечения сердечно-сосудистых заболеваний. Ожидаемые результаты 2020: изучение эффектов аблации на изолированных тканях. Изучение результатов аблации in vivo на здоровых животных. 2021: эксперименты на моделях легочной гипертензии, артериальной гипертензии у животных. 2022: эксперименты на модели фибрилляции предсердий. Обработка полученных данных.
Научный руководитель: д.м.н. Михайлов Евгений Николаевич
Ответственный исполнитель: к.м.н., Гончарова Наталья Сергеевна
Состояние вопроса: Денервация легочной артерии (ДЛА) снижает давление в ЛА. Ранее был предложен подход к селективной абляции ЛА: стимуляционное картирование ЛА — метод определения зон безопасной и эффективной денервации ЛА. Необходима разработка подходов к адаптации глубины повреждения участков ЛА на основании картирования, что может быть достигнуто комбинацией источников энергии (радиочастотный (РЧ) ток и лазер), а также управлением параметрами аппликаций. Научные подходы: эксперименты на свиньях с радиочастотной и лазерной аблацией ЛА в зоне ее бифуркации на различных параметрах аблации, будет изучена глубина и гомогенность 2020—1902-01-0593 25.05.2020 19:16 8 1ec81aa0fc2a6d747160e4d1b335eb8c повреждения периваскулярных нервов и самой ЛА. После изучения результатов на здоровых животных будет изучена адаптированная аблация ЛА на острой модели легочной гипертензии, а также изучены эффекты в хроническом эксперименте. Новизна. Подход к адаптированной денервации ЛА на основании комбинирования: стимуляционного картирования ЛА, модификации глубины повреждения на разных участках ЛА с использованием различных источников энергии. Ожидаемые результаты: 2020: эксперименты с лазерной и РЧ аблацией ЛА на изолированной ткани и in vivo. 2021: разработка адаптированной денервации ЛА на модели острой легочной артериальной гипертензии. 2020: хронический эксперимент денервации с моделированием легочной гипертензии.
Научный руководитель: акад. РАН д.м.н. Шляхто Евгений Владимирович
Ответственный исполнитель: д.м.н. Мамонтов Олег Викторович
Состояние вопроса: данные о степени и динамике реиннервации трансплантированного сердца противоречивы. Неизвестно, как этот процесс сопряжен с восстановлением толерантности к нагрузке. Научные подходы: оценка вегетативной иннервации через 6 недель после хирургической денервации и трансплантации сердца гистохимическими и физиологическими методами в эксперименте. Оценка результатов кардиореспираторного теста и автономной регуляции после трансплантации сердца у людей. Ожидаемые результаты 2020: модель денервации и ортоптической трансплантации сердца, данные обследования пациентов с терминальной СН до и после трансплантации 2021: данные по динамике реиннервации сердца в эксперименте. 2022: данные по динамике реиннервации и толерантности к нагрузке у пациентов после трансплантации.
Научный руководитель: д.м.н. проф. Ситникова Мария Юрьевна
VIII. Новости
IX. Публикации
Neurohumoral, cardiac and inflammatory markers in the evaluation of heart failure severity and progression. Polyakova EA, Mikhaylov EN, Sonin DL, Cheburkin YV, Galagudza MM. J Geriatr Cardiol. 2021 Jan 28;18 (1):47-66. doi: 10.11909/j.issn.1671—5411.2021.01.007.PMID: 33613659
Dual-energy computed tomography-angiography in the evaluation and management of significant multiple pulmonary vein stenoses following atrial fibrillation ablation. Simakova MA, Karpova DV, Marukyan NV, Pishchulov KA, Mikhaylov ENM, Moiseeva OM. Pulm Circ. 2020 Dec 6;10 (4):2045894020969499. doi: 10.1177/2045894020969499. eCollection 2020 Oct-Dec.PMID: 33335709
Stimulation Mapping of the Pulmonary Artery for Denervation Procedures: an Experimental Study.
Animal model of assessing cerebrovascular functional reserve by imaging photoplethysmography. Mamontov OV, Sokolov AY, Volynsky MA, Osipchuk AV, Zaytsev VV, Romashko RV, Kamshilin AA. Sci Rep. 2020 Nov 4;10 (1):19008. doi: 10.1038/s41598-020-75824-w.
Condori Leandro HI, Vakhrushev AD, Goncharova NS, Korobchenko LE, Koshevaya EG, Mitrofanova LB, Andreeva EM, Moiseeva OM, Lebedev DS, Mikhaylov EN. J Cardiovasc Transl Res. 2020 Oct 27. doi: 10.1007/s12265-020-10079-4. Online ahead of print.
Model of Chronic Thromboembolic Pulmonary Hypertension in Rats Caused by Repeated Intravenous Administration of Partially Biodegradable Sodium Alginate Microspheres. Karpov AA, Anikin NA, Mihailova AM, Smirnov SS, Vaulina DD, Shilenko LA, Ivkin DY, Bagrov AY, Moiseeva OM, Galagudza MM. Int J Mol Sci. 2021 Jan 24;22 (3):1149. doi: 10.3390/ijms22031149.
Gap19, a Cx43 Hemichannel Inhibitor, Acts as a Gating Modifier That Decreases Main State Opening While Increasing Substate Gating. Lissoni A, Wang N, Nezlobinskii T, De Smet M, Panfilov AV, Vandersickel N, Leybaert L, Witschas K. Int J Mol Sci. 2020 Oct 5;21 (19):7340. doi: 10.3390/ijms21197340.
